Bài tập cân bằng phương trình Al2(SO4)3 + NaOH = Na2SO4+NaAlO2+H2O là một bài tập khó với đại đa số các bạn học sinh. Với bài viết ngày hôm nay chúng ta hãy cùng nhau giải bài tập này nhé. Nhưng để giả bài tập này chúng ta cũng cần nên cùng ôn lại 1 số phương pháp giải bài tập cân bằng này nhé.
Cách cân bằng Phương trình Hóa học
Đối với bộ môn Hóa học thì việc phải cân bằng những phương trình luôn là nỗi ám ảnh của các bạn học sinh. Nhưng thực ra việc cân bằng những phương trình hóa học này thật rất là đơn giản. Tuy nhiên, có những phương trình mà ở đó nhiều chất tham gia phản ứng và cho ra nhiều sản phẩm làm cho các bạn học sinh khi gặp phải đề khó sẽ bị rối không thể cân bằng được phương trình. Dưới đây là một số những phương pháp cân bằng phương trình giúp các bạn học sinhcó thể làm được những bài tập cân bằng phương trình hóa học một cách dễ dàng, nhanh chóng và chính xác nhất.
Trước hết các bạn học sinh cần ghi nhớ trình tự cân bằng một phương trình Hóa học:
Bước thứ 1: cân bằng nhóm nguyên tử (OH, NO3, SO4, CO2, PO4..)
Bước thứ 2: cân bằng nguyên tử Hidro
Bước thứ 3: cân bằng nguyên tử Oxi
Bước thứ 4: cân bằng các nguyên tố còn lại.
Cân bằng theo phương pháp truyền thống
Cách thực hiện:
Viết phương trình đã cho. Ở ví dụ này, bạn sẽ có:
- C3H8 + O2 –> H2O + CO2
- Phản ứng này xảy ra khi prôban (C3H8) được đốt cháy trong ôxy để tạo thành nước và cacbon điôxít.
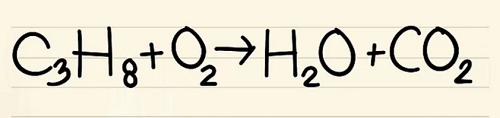
Bước 1:
Viết số lượng nguyên tử của mỗi nguyên tố mà bạn có ở mỗi bên phương trình. Xem các chỉ số dưới bên cạnh mỗi nguyên tử để tìm ra số lượng nguyên tử trong phương trình.
- Bên trái: 3 cacbon, 8 hyđrô và 2 ôxy.
- Bên phải: 1 cacbon, 2 hyđrô và 3 ôxy.
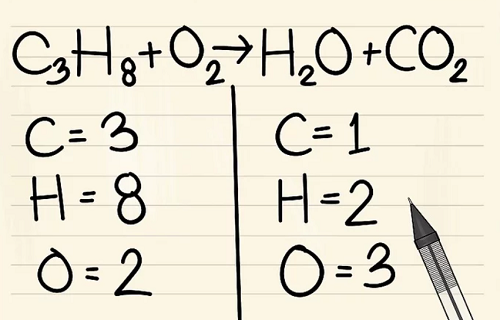
Bước 2:
Luôn để hyđrô và ôxy cuối cùng
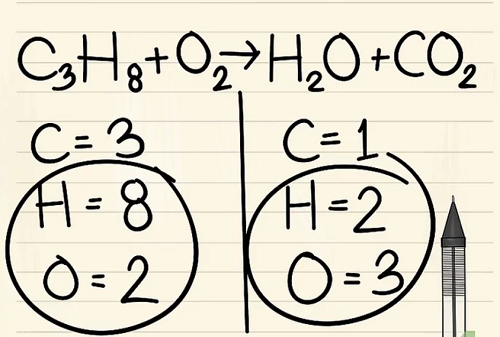
Bước 3:
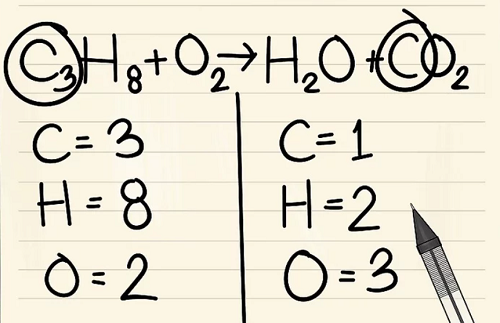
Nếu bạn còn lại nhiều hơn một nguyên tố để cân bằng: hãy chọn nguyên tố xuất hiện chỉ trong phân tử đơn của chất phản ứng và chỉ trong phân tử đơn của sản phẩm. Điều này có nghĩa rằng bạn sẽ cần phải cân bằng các nguyên tử cacbon trước.
Bước 4:
Thêm hệ số cho đơn nguyên tử cacbon vào bên phải của phương trình để cân bằng nó với 3 nguyên tử cacbon ở bên trái của phương trình.
- C3H8 + O2 –> H2O + 3CO2
- Hệ số 3 đứng trước cacbon ở phía bên phải chỉ ra có 3 nguyên tử cacbon giống như chỉ số dưới 3 ở phía bên trái cho biết có 3 nguyên tử cacbon.
- Trong phương trình hóa học, bạn có thể thay đổi hệ số, nhưng không thể thay đổi chỉ số dưới.

Bước 5:
Tiếp đến là cân bằng nguyên tử hyđrô. Bạn có 8 nguyên tử hyđrô ở bên trái. Do đó bạn sẽ cần có 8 ở bên phải.
C3H8 + O2 –> 4H2O + 3CO2
Ở bên phải giờ bạn thêm 4 làm hệ số vì chỉ số dưới cho biết bạn đã có 2 nguyên tử hyđrô.
Khi bạn nhân hệ số 4 với chỉ số 2, bạn có 8.
6 nguyên tử Ôxy khác là từ 3CO2.(3×2=6 nguyên tử ôxy+ 4 nguyên tử ôxy khác=10)

Bước 6:
Cân bằng các nguyên tử ôxy.
- Bởi vì bạn đã thêm hệ số vào các phân tử bên phải phương trình nên số nguyên tử ôxy đã thay đổi. Giờ bạn có 4 nguyên tử ôxy trong phân tử nước và 6 nguyên tử ôxy trong phân tử cacbon điôxít. Tổng cộng ta có 10 nguyên tử ôxy.
- Thêm hệ số 5 vào phân tử ôxy ở bên trái phương trình. Giờ bạn có 10 phân tử ôxy ở mỗi bên.
- C3H8 + 5O2 –> 4H2O + 3CO2.
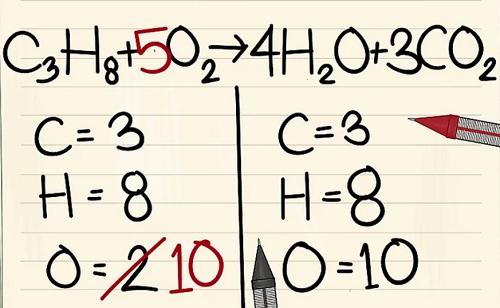
Kết quả
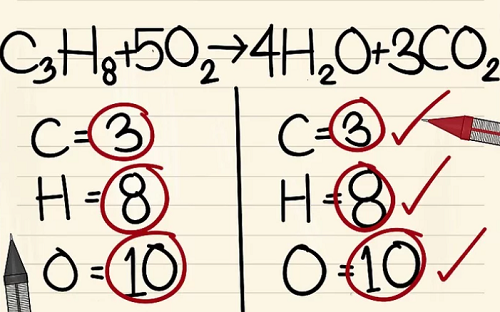
Cân bằng theo trình tự Kim loại – Phi kim
Cân bằng phương trình hóa học theo trình tự Kim loại – Phi kim có nghĩa là chúng ta sẽ cân bằng theo trình tự cân bằng số nguyên tử của kim loại trước rồi tới phi kim, sau đó tới Hidro và tới oxi.
Vd: CuFeS2 + O2 -> CuO + Fe2O3 + SO2
Do nguyên tử Cu đã cân bằng nên thứ tự cân bằng đầu tiên sẽ là: Fe sau đó sẽ là Cu, S, O rồi nhân đôi các hệ số ta có kết quả là:
4CuFeS2 + 13O2 = 4CuO + 2 Fe2O3 + 8SO2
Phương pháp cân bằng phương trình chẵn lẻ
Đây là một trong những cách thức có thể cân bằng phương trình hóa học dễ dàng và nhanh chóng được sử dụng phổ biến. Với phương pháp này các bạn học sinh có thể sử dụng phương pháp chẵn lẻ, được áp dụng như sau:
- Khi mà một phương trình phản ứng đã cân bằng có nghĩa là số nguyên tử của nguyên tố ở vế phải sẽ bằng với số nguyên tử của nguyên tố ở vế trái, đồng nghĩa là số nguyên tử của một nguyên tố ở vế trái chẵn thì số nguyên tử của nguyên tố đó ở vế phải cũng phải chẵn.
- Cho nên nếu trong phương trình mà nếu một trong số những số nguyên tử của bất kỳ nguyên tố nào còn lẻ thì phải nhân đôi.
Vd: Ta lấy lại ví dụ ở trên: Fe + O2 -> Fe2O3
Vế trái số nguyên tử của Fe lẻ còn bên phải thì chẵn nên ta nhân Fe ở vế trái lên 2. Còn oxi ở vế trái thì chẵn, vế phải thì lẻ, nên ta cũng nhân 2 cho số nguyên tử oxi ở vế phải.
2Fe + O2 -> 2Fe2O3
Đến đây số nguyên tử của cả 2 bên đều đã chẵn, ta chỉ việc cân bằng lại cho sô nguyên tử của 2 bên bằng nhau.
4Fe + 3O2 = 2Fe2O3
Phương pháp từ nguyên tố chung nhất
Phương pháp từ nguyên tố chung nhất có nghĩa là nguyên tố nào có mặt trong hầu hết các hợp chất trong phương trình cần cân bằng thì chúng ta sẽ chọn để cân bằng hệ số các phân tử trước.
Vd: Cu + HNO3 -> Cu(NO3)2 + NO + H20
Trong phương trình này, nguyên tố Oxi xuất hiện nhiều nhất trong hầu hết các hợp chất nên sẽ cân bằng Oxi trước, rồi tới các nguyên tố khác.
Vế trái có 8 oxi, vế phải có 3 oxi. Vậy bội số chung nhỏ nhất của 8 và 3 là 24, suy ra hệ số của HNO3 là 24/3=8
Vậy phản ứng cân bằng là: 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
Phương pháp cân bằng phương trình bằng cách dùng hệ số thập phân
Phương pháp này áp dụng như sau: đặt hệ số vào các chất tham gia phản ứng, có thể là số nguyên tố hoặc là phân số miễn sao cho số nguyên tử ở cả hai vế đều bằng nhau. Sau đó nhân lên để khử mẫu số chung ở 2 vế.
Vd: Fe + O2 -> Fe2O3
Trước tiên ta thêm hệ số vào sẽ thành : 2Fe + 3/2O2 -> Fe2O3
Lúc này số nguyên tử ở 2 vế đã bằng nhau. Sau đó chúng ta nhân lên để khử mẫu, ở phương trình sẽ nhân lên cho 2.
Kết quả là: 4Fe + 3O2 = 2Fe2O3
Phương pháp cân bằng phương trình bằng đại số
Học sinh đặt hệ số a, b, c… lần lượt vào các công thức ở 2 vế của phương trình và thiết lập các phương trình toán học chứa các ẩn trên theo nguyên tắc số nguyên tử của nguyên tố trước và sau phản ứng bằng nhau. Bạn sẽ được 1 hệ phương trình chứa các ẩn, giải hệ phương trình này và đưa hệ số tương ứng tìm dược vào phương trình phản ứng và khử mẫu (nếu cần).
Với bài toán cân bằng phương trình hóa học FeS2 + O2 –> Fe2O3 + SO2, ta thấy, ở vế trái số nguyên tử O2 là chẵn với bất kỳ hệ số nào trong khi đó vế phải, trong SO2 oxi là chẵn nhưng trong Fe2O3 là lẻ nên phải nhân đôi. Từ đó cân bằng tiếp các hệ số còn lại. 2Fe2O3 –> 4FeS2 –> 8SO2 + 11O2, thay vào PTPU ta được phương trình cân bằng là 4FeS2 + 11O2 = 2Fe2O3 + 8SO2.
Cân bằng phương trình Al2(SO4)3 + NaOH = Na2SO4+NaAlO2+H2O
Al2(SO4)3 là gì?
Al2(SO4)3 hay còn gọi là Nhôm sunfat với công thức hóa học rút gọn là công thức rút gọn Al2O12S3. Bạn đã bao giờ tự hỏi làm thế nào chúng ta quản lý được nước uống quan toàn chảy ra từ vòi nước của chúng ta? Câu trả lời là bạn có thể dùng nhôm sunfat.
Một trong những ứng dụng khác của Al2(SO4)3 (nhôm sunfat) là nhuộm và in trên vải. Khi hòa tan trong một lượng lớn nước có độ pH trung tính hoặc hơi kiềm, hợp chất này tạo ra một chất dính, nhôm hydroxit.
Trong quá khứ, Al2(SO4)3 (nhôm sunfat đã được sử dụng để sản xuất giấy, mặc dù các tác nhân tổng hợp hầu hết đã thay thế nó. Nhôm sunfat giúp định cỡ giấy.
Trong lĩnh vực y tế, Al2(SO4)3 (nhôm sunfat được sử dụng như một chất làm đông để điều trị vết cắt và trầy xước nhỏ cũng như chất khử mùi (do đặc tính kháng khuẩn của nó).
Giải thích chi tiết phương trình Al2(SO4)3 tác dụng cùng NaOH
Điều kiện phản ứng của Al2(SO4)3 + NaOH
- Không có điều kiện gì đặc biệt khi Al2(SO4)3 kết hợp với NaOH
Al2(SO4)3 + NaOH xảy ra hiện tượng
- Phương trình không có hiện tượng nhận biết đặc biệt.
- Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm Na2SO4 (natri sulfat), NaAl(OH)4 (Sodium tetrahydroxyaluminate), được sinh ra
- Hoặc bạn phải quan sát chất tham gia Al2(SO4)3 (Nhôm sunfat), NaOH (natri hidroxit) (trạng thái: đậm đặc), biến mất.
Bài giải về cân bằng phương trình Al2(SO4)3 + NaOH = Na2SO4+NaAlO2+H2O
| Al2(SO4)3 | + | 8NaOH | → | 3Na2SO4 | + | 2NaAl(OH)4 |
| Nhôm sunfat | natri hidroxit (đậm đặc) | natri sulfat | Sodium tetrahydroxyaluminate | |||
| Muối | Ba zơ | Muối |
Mong rằng với bài tập giải về cân bằng phương trình Al2(SO4)3 + NaOH = Na2SO4+NaAlO2+H2O sẽ giúp các bạn nhiều hơn trong việc giải các bài tập khác. Mong rằng nỗi ám ảnh về giải phương trình cân bằng của bạn sẽ không còn nữa nhé.
[content_block id=1317]